Μάθημα : Χημεία Προσανατολισμού - Κεφάλαιο 6 (Μέρος Ε')
Κωδικός : 1251060412
1251060412 - ΜΙΧΑΗΛ ΣΜΑΡΑΓΔΑΚΗΣ
Περιγραφή Μαθήματος
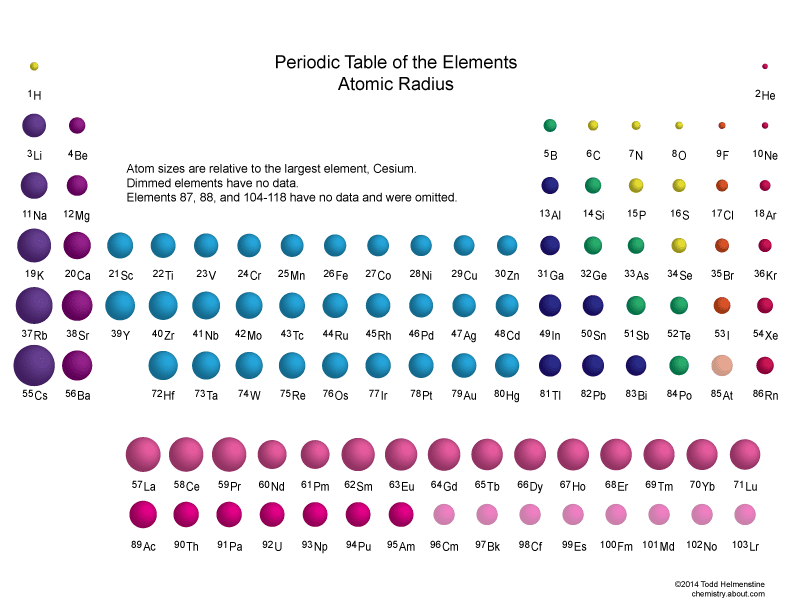
Μεταβολή ιδιοτήτων χημικών στοιχείων:
Ατομική Ακτίνα
Ενέργεια Ιοντισμού
Ηλεκτραρνητικότητα
Η Ατομική Ακτίνα που περιγράφει το μέγεθος ενός ατόμου καθορίζεται από τα ηλεκτρόνια της εξωτερικής στοιβάδας του.

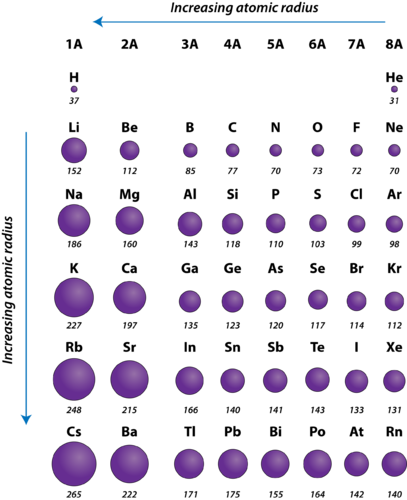
Η Ατομική Ακτίνα των στοιχείων της ίδια περιόδου αυξάνεται από δεξιά προς αριστερά.
Καθώς προχωράμε προς τα δεξιά στον περιοδικό πίνακα κάθε στοιχείο έχει 1 επιπλέον πρωτόνιο στον πυρήνα του με αποτέλεσμα να έλκονται τα ηλεκτρόνια του πιο ισχυρά από αυτόν και να βρίσκονται πιο κοντά του, μειώνοντας την ατομική ακτίνα. Φυσικά υπάρχει κι ένα επιπλέον ηλεκτρόνιο στο κάθε άτομο, αλλά η ύπαρξη του δεν μπορεί να αντισταθμίσει πλήρως την επιπλέον έλξη του πυρήνα, ειδικά στις κύριες ομάδες όπου το ηλεκτρόνιο τοποθετείται στην εξωτερική στοιβάδα. Στις δευτερεύουσες ομάδες η διαφορά είναι μικρότερη ενώ παρατηρούνται και κάποιες εξαιρέσεις καθώς τα ηλεκτρόνια τοποθετούνται σε εσωτερική στοιβάδα, ενώ υπάρχουν και οι αναδιατάξεις ηλεκτρονίων στις ομάδες d4 και d9 αλλά τέτοιες εξαιρέσεις δεν θα μας απασχολήσουν.
Η Ατομική Ακτίνα των στοιχείων της ίδια ομάδας αυξάνεται από πάνω προς τα κάτω.
Καθώς προχωράμε προς τα κάτω στον Περιοδικό Πίνακα ο Κύριος Κβαντικός Αριθμός της εξωτερικής στοιβάδας αυξάνεται, και κατά συνέπεια και το ηλεκτρονιακό νέφος της. Τα ηλεκτρόνια της έχουν μεγαλύτερη ενέργεια κι έτσι βρίσκονται κατά μέσο όρο πιο μακριά από τον πυρήνα.
Ημερολόγιο
Ανακοινώσεις
Όλες...- - Δεν υπάρχουν ανακοινώσεις -